
|
Science » » Przyszłość komórek macierzystych w medycynie [3] Seria innych eksperymentów polegała na wstrzyknięciu nerwowych komórek macierzystych do kurzych i mysich embrionów. Komórki macierzyste śledzono za pomocą specjalnego znacznika, który można było zauważyć jako niebieskie barwienie. (Ryc. 5) 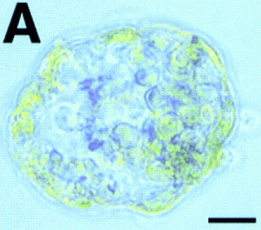 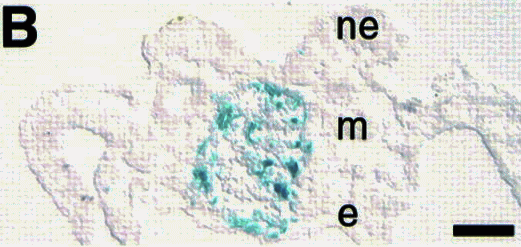 Rycina 5. Wybarwione na niebiesko nerwowe komórki rozpoczynają swoją wędrówkę po wstrzyknięciu do embrionu mysiego (A) i kurzego (B). Na zdjęciu oznaczono warstwy: ne — neuroektorderma, m — mezoderma i e — endoderma. [22] [ 1 ] W obu przypadkach komórki potomne z iniekcji znalazły się w wielu tkankach gospodarza wystawione na działanie różnych czynników stymulujących do różnicowania. Okazało się, że zintegrowały się one całkowicie z nowymi tkankami, będąc morfologicznie nierozróżnialne. Jedynie dzięki specjalnym znacznikom udało się je zidentyfikować (Ryc. 6 i 7). Dały one początek tkankom takim jak wątroba, komórki mięśniowe czy epiderma, czyli komórkom należącym do wszystkich trzech warstw zarodkowych.[22] 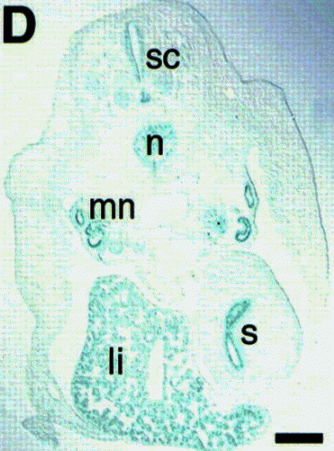 Rycina 6. Stadium embrionalne kury (przekrój poprzeczny) z wybarwionymi na niebiesko komórkami macierzystymi. Na zdjęciu zaznaczono m.in.: sc - rdzeń kręgowy, n — struna grzbietowa, li — wątroba, s — żołądek. [22] [ 1 ] 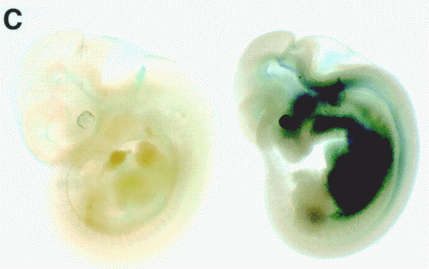 Rycina 7. Porównanie mysiego embrionu: po lewej normalny embrion, po prawej chimera po wstrzyknięciu nerwowych komórek macierzystych. Niebieskie i ciemnozielone kolory wykrywają ich obecność. [22] [ 1 ] Co siedzi jeszcze pod skórą?Okazuje się, że komórki skórne — fibroblasty biorą udział w formowaniu nowych włókien mięśniowych, po transplantacji do regenerującego się mięśnia.[24] W Europie prowadzi się już próby kliniczne regeneracji ludzkiego rdzenia kręgowego po urazach. Komórki macierzyste pobierane są z komory nosowej i przeszczepiane w region uszkodzonego rdzenia podczas jednego zabiegu chirurgicznego. Terapia wydaje się obiecująca w rekonwalescencji niedawnych urazów. Podsumowanie: wielka szansa czy złudne nadzieje?Powyższe badania podważyły długo panujący dogmat o braku zdolności przekształcania dorosłych komórek macierzystych w linie komórkowe niespecyficzne dla danej tkanki. Uważano, że komórki przechodzą przemiany wyłącznie w jednym kierunku bez możliwości zmiany losu. Rozwój badań nad tą kwestią spowodował spore sukcesy i mnóstwo publikacji. O ile większość doświadczeń została przeprowadzona na myszach, istnieją również przypadki sugerujące podobny fenomen w takich organizmach jak muszka owocowa czy człowiek. Według klasycznego modelu komórka dzieli się podążając ścisłą drogą pomiędzy kolejnymi pokoleniami komórek, prowadząc do powstania dwóch potomnych komórek macierzystych — prekursorów, które dalej odpowiednio stymulowane zamieniają się w dwie niezależne, wyspecjalizowane linie komórkowe. Według Jonasa Frisena wyróżnić można trzy główne drogi niespodziewanej zmiany losu komórek macierzystych.[23] (Ryc. 8) Pierwszym z nich jest transróżnicowanie (ang. transdifferentiation), które zachodzi, kiedy w pełni zróżnicowana komórka przejmuje fenotyp innej zróżnicowanej komórki, często bez podziału. Inny proces zwany transdeterminacją (ang. transdetermination) polega na zmianie właściwości pomiędzy dwiema komórkami macierzystymi bądź prekursorami. Trzecia droga to deróżnicowanie (ang. dedifferentiation), czyli zmiana prekursora w pierwszą generację komórek macierzystych i zróżnicowanie w zupełnie inną linię. 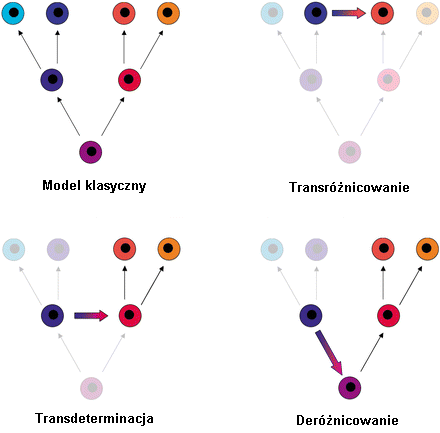 Rycina 8. Proponowane rodzaje dróg ku zmianie tożsamości komórkowej. [23] [ 2 ] W ostatnich latach pojawiły się również wątpliwości świadczące o innym charakterze notowanych przemian i sprowokowały dyskusję nad interpretacją wyników. Okazuje się, że część procesów uważana za plastyczność komórek macierzystych mogła być przypisana zupełnie innym, niedawno poznanym procesom. Po pierwsze, wiele doświadczeń prowadzonych było w warunkach nienaturalnych, często czysto eksperymentalnych — na przykład ASC wstrzyknięte zostały do zwierzęcych embrionów. Ich celem była raczej wnikliwa analiza samych komórek niż symulacja warunków fizjologicznych. Problem w tym, że nie wszystko co działa in vitro będzie działać in vivo. Wielu naukowców podważa również naturalne istnienie MAPC, które wydają się jednym z najbardziej znaczących sukcesów w poszukiwaniu plastyczności u ASC. Uważa się, że mogą one być skutkiem hodowli, nie ma jednoznacznego dowodu, że występują one in vivo. [1] Poza tym większość znaczących efektów zaobserwowana została w warunkach patologicznych, po podrażnieniu, uszkodzeniu lub osłabieniu ustroju. Czy fakt wymuszonej adaptacji wstrzykniętych komórek nie przekłamuje zbyt entuzjastycznych wyników? Przypadki plastyczności ASC podczas normalnego rozwoju są znacznie mniej liczne, jednak obecne — na przykład nerwowa ektoderma daje początek mezodermalnym pochodnym, innym przykładem są płytki epidermalne, zgrubienia prymitywnej skóry, które mogą powstać z leżącej poniżej warstwy nerwowej. Istnieje kilka sugestii w jaki sposób pewne procesy mogą przekłamać wyniki doświadczeń. Jedną z nich jest niehomogeniczność źródła — jest bardzo prawdopodobne, że komórki używane do doświadczeń mogły zawierać nie tylko komórki jednego rodzaju. Na przykład komórki szpiku kostnego użyte do iniekcji mogły zawierać rezydujące w nim prekursory mięśniowych czy wątrobowych komórek.. Innym powodem nadinterpretacji może być zbyt intensywne namnażanie komórek na pożywkach — mogą one tworzyć wtedy odrębne linie i posiadać zupełnie inną charakterystykę. Wreszcie wspominana wyżej fuzja komórek może być w dużym stopniu mylnie identyfikowana z plastycznością ASC. Proces ten polega na zlaniu się dwóch komórek, które są w stanie przywrócić fizjologiczną równowagę poprzez odrzucenie nadkompletu chromosomów. Jednak marker genetyczny może pozostać i wskazywać, że komórka macierzysta uległa zróżnicowaniu. W rzeczywistości zaś nastąpiło połączenie komórek, które bynajmniej nie świadczy o plastyczności badanych komórek macierzystych. (Ryc. 9) 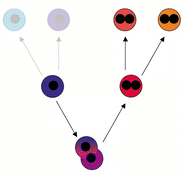 Rycina 9. Przykład fuzji komórek, która może być przyczyną błędnej identyfikacji i przypisaniu komórkom macierzystym plastyczności. [23] [ 2 ] Naukowcy uważają, że na obecnym etapie nowe badania powinny być przyjmowane na równi z entuzjazmem jak i sceptycyzmem. Nie jesteśmy na razie w stanie stwierdzić jednoznacznie, czy wyniki badań są rzeczywistym dowodem na plastyczność dorosłych komórek macierzystych, czy artefaktem na skutek wyżej wspomnianych procesów. Badania nad komórkami macierzystymi są obecnie jedną z najbardziej atrakcyjnych dziedzin w biologii eksperymentalnej, możemy spodziewać się więc znacznych postępów jeszcze w tej dekadzie. Naukowcy mają w swoim ręku potężne narzędzia jakie ofiaruje im biologia molekularna, należy się tylko zastanowić jak je użyć. Wydaje się, że problem etyczny związany z manipulacjami genetycznymi pozostanie przez jeszcze długi czas nierozwiązany, dlatego przełomowe odkrycia w kwestii ASC są bardzo pożądane i powinny pogodzić obie strony konfliktu, łącząc je w jeden cel: dobro ludzkości. * Literatura:
Footnotes: [ 2 ] Przedrukowane i zmodyfikowane z: „Stem Cell Plasticity?"
by Jonas Frisen, Neuron 2002, Vol. 35, 415-18, Copyright © 2002,
za zgodą Elsevier. (Ref # HW/jb/jun04.j016) « (Published: 12-06-2004 Last change: 19-06-2004)
page 3443 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| [ Cooperation ] [ Advertise ] [ Map of the site ] [ F.A.Q. ] [ Store ] [ Sign up ] [ Contact ] The Rationalist © Copyright 2000-2018 (English section of Polish Racjonalista.pl) | ||



 Ukończył biologię molekularną na Uniwersytecie Adama Mickiewicza w Poznaniu. Pracował jako Research Specialist in Health Science w Department of Anatomy and Cell Biology na University of Illinois w Chicago. Obecnie pracuje jako Associate Cell Biologist / Histologist w Abbott Laboratories (Illinois). Specjalizuje się w ekspresji białek 'od zera', hodowlach linii komórkowych, symulacji in vitro procesów zachodzących w komórkach. Jego pasją jest teoria ewolucji, w szczególności ewolucja systemów biochemicznych i pochodzenie życia we Wszechświecie.
Ukończył biologię molekularną na Uniwersytecie Adama Mickiewicza w Poznaniu. Pracował jako Research Specialist in Health Science w Department of Anatomy and Cell Biology na University of Illinois w Chicago. Obecnie pracuje jako Associate Cell Biologist / Histologist w Abbott Laboratories (Illinois). Specjalizuje się w ekspresji białek 'od zera', hodowlach linii komórkowych, symulacji in vitro procesów zachodzących w komórkach. Jego pasją jest teoria ewolucji, w szczególności ewolucja systemów biochemicznych i pochodzenie życia we Wszechświecie.